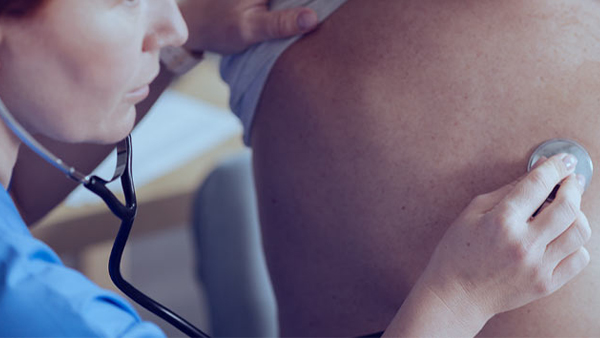
Detección de la fibrosis pulmonar en imágenes por TCAR
En el diagnóstico de las enfermedades pulmonares intersticiales difusas (EPID), la tomografía computarizada de alta resolución (TCAR) es el gold estándar1-3
La TCAR ofrece información útil para el diagnóstico acerca de:2-7
Extensión de la fibrosis pulmonar2,6
.png)
Características fibróticas y patrones fibróticos3-5
Características inflamatorias4

Otras manifestaciones torácicas de las enfermedades autoinmunes sistémicas (EAS)7
Solicitud de TCAR
Al solicitar una TCAR, es necesario indicar que el paciente está siendo evaluado para una EPID,8,9 por lo que se ha de utilizar un protocolo de screening apropiado para EPID3,9-11
Además de proporcionar al radiólogo toda la información relevante del paciente:9,12

Evaluación de la TCAR
Las principales características radiológicas de fibrosis pulmonar detectadas en la TCAR incluyen:8,13
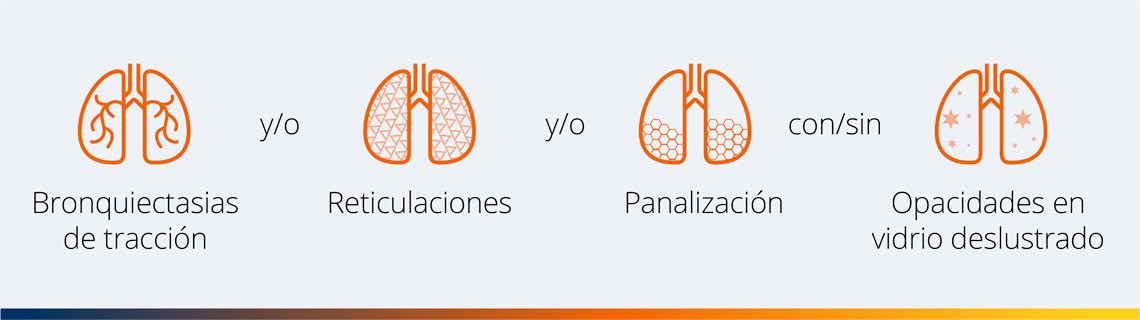
La evaluación de las imágenes en TCAR va dirigida a la detección de los patrones fibróticos más comunes:14
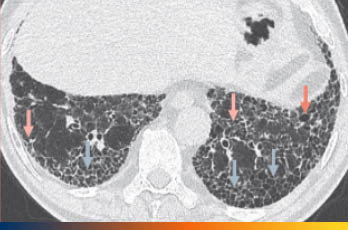
Características del patrón típico NIU:8-10,15
- Distribución basal subpleural heterogénea
- Opacidades en vidrio deslustrado moderadas
- Panalización
- Patrón reticular con bronquiectasias de tracción periféricas o bronquiolectasias
El patrón NIU se ha asociado con un peor pronóstico en algunas EPI-EAS16-21

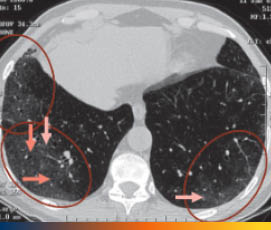
Características del patrón NINE:8,22,23
- Distribución basal subpleural homogénea
- Preservación subpleural
- Opacidades en vidrio deslustrado
- Sin panalización o muy poco común
- Reticulación
- Bronquiectasias de tracción o bronquiolectasias
- Pérdida de volumen del lóbulo inferior

La dosis de radiación efectiva estimada de una TCAR estándar es 2–4 mSv, menor que la dosis efectiva estimada de un examen torácico diagnóstico de rutina (estimado 5–7 mSv).24
Dosis de radiación efectiva para exposición ambiental y diferentes protocolos de imágenes de tórax24
| Dosis efectiva (mSv) |
Radiación de fondo equivalente (mSv) | Referencia(s) | Fecha de publicación | |
| Exposición anual de la radiación de fondo en EEUU |
3,1 | Ref | Wakeford | 2008 |
| Exposición anual de las tripulaciones de las aerolíneas en vuelos de larga distancia |
2-3 | 0,66-1,0 | Bagshaw | 2008 |
| Límite de exposición anual permisible para trabajadores de radiación (incluidos radiólogos, técnicos radiológicos y físicos médicos) |
50 | - | United States Nuclear Regulatory Commission, International Commission on Radiological Protection |
2008, 2019 y 2007 |
| Radiografía torácica | 0,02-0,1 | - | Mettler et al. | 2008 |
| TC para la detección de cáncer de pulmón de dosis baja |
1-2 | - | Larke, et al. American Association of Physicists in Medicine |
2011 y 2019 |
| TC de tórax de diagnóstico de rutina |
5-7 | - | Larke, et al. | 2011 |
| Protocolo estándar para TCAR torácica (valor de referencia) |
1,6-4,0 | 0,54-1,30 | Katsura, et al. Pontana, et al.Frauenfelder, et al. Winklehner, et al. |
2012 2016 2014 2012 |
| Reconstrucción iterativa afirmada por sinograma y dosis reducida |
1,8 | 0,58 | Pontana, et al. | 2016 |
| Reconstrucción iterativa basada en modelo y dosis reducida |
0,85 | 0,28 | Katsura, et al. | 2012 |
| Protocolo de 9 cortes | 0,08 | 0,02 | Frauenfelder, et al. | 2014 |
| Protocolos de incrementos de 10 mm, 7 cortes y 3 cortes |
0,014-0,154 | 0,004-0,049 | Winklehner, et al. | 2012 |
Khanna D, et al. J Scleroderma Relat Disord. 2022;7(3):168-178.
Curso de TMC Academy con casos clínicos y sesiones online sobre radiología en EPID asociada a EAS
Atlas digital de imágenes de patrones radiológicos e histopatológicos de EPID.
Signos de EPID en la auscultación
Reconoce los distintos sonidos que puedes identificar en la auscultación pulmonar para diagnosticar las enfermedades pulmonares intersticiales.
EPID: enfermedades pulmonares intersticiales difusas; EPI-EAS: EPID asociada a enfermedades autoinmunes sistémicas; EAS: enfermedades autoinmunes sistémicas; FPI: fibrosis pulmonar idiopática; NINE: neumonía intersticial no específica; NIU: neumonía intersticial usual; TC: tomografía computarizada; TCAR: tomografía computarizada de alta resolución.
Referencies
- Khanna D, et al. J Scleroderm Relat Dis 2022;
- Geerts S, et al. Sarcoidosis Vasc Diffuse Lung Dis 2017;34:326–35;
- Chung J, et al. J Vis Exp 2020;160:e60300;
- Chiu Y-H, et al. Respir Med 2021;187:106579;
- Jacob J, Hansell DM. Respirology 2015;20:859–72;
- Sverzellati N. Respir Res 2013;14(Suppl 1):S3;
- Mira-Avendano I, et al. Mayo Clin Proc 2019;94:309–25;
- Gotway MB, et al. Thorax 2007;62:546–53;
- Chung JH, Goldin JG. Lung 2018;196:561–7;
- Raghu G, et al. Am J Respir Crit Care Med 2018;198:e44–68;
- Prosch H, et al. Eur Radiol 2012;23:1553–63;
- Castillo C, et al. J Med Radiat Sci 2021;68:60–74;
- Torres PPTES, et al. J Bras Pneumol 2021;47:e20200096;
- Wells AU, et al. Eur Respir J 2018;51:1800692;
- Raghu G, et al. Am J Respir Crit Care Med 2011;183:788–824;
- Solomon JJ, et al. Eur Respir J 2016;47:588–96;
- Kim EJ, et al. Eur Respir J 2010;35:1322–8;
- Yunt ZX, et al. Respir Med 2017;126:100–4;
- Kelly CA, et al. Rheumatology (Oxford) 2014;53:1676–82;
- Marie I, et al. Arthritis Rheum 2011;63:3439–47;
- Cobo-Ibáñez T, et al. Clin Rheumatol 2019;38:803–15;
- Kligerman SJ, et al. Radiographics 2009;29:73–87; 2
- Hansell DM, et al. Radiology 2008;246:697–722;
- Khanna D, et al. J Scleroderma Relat Disord. 2022;7(3):168-178.
ILD.0858.032023