Estudio SENSCIS®

Objetivo del estudio1
El estudio SENSCIS® evaluó la eficacia y la seguridad de nintedanib en pacientes con enfermedad pulmonar intersticial asociada a esclerosis sistémica (EPI-ES) (NCT02597933).1
Diseño del estudio1,2
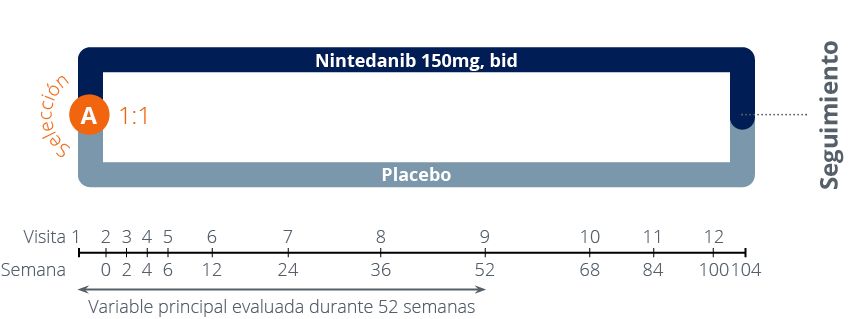
Ensayo clínico de fase III, aleatorizado, doble ciego, controlado con placebo y de grupos paralelos. Se aleatorizaron 576 pacientes en una proporción 1:1 para recibir nintedanib o placebo. Se llevó a cabo en 32 países durante un periodo de, al menos, 52 semanas. Los pacientes se mantuvieron en tratamiento ciego hasta que el último sujeto llegó a la semana 52, pero durante no más de 100 semanas.1,2
El criterio principal de valoración se evaluó a las 52 semanas.
Principales criterios de inclusión1
- 18 años o más
- Diagnóstico de esclerosis sistémica*3
- EPID confirmada mediante TCAR torácica realizada en los 12 meses previos al cribaje y con extensión de la fibrosis pulmonar ≥10%
- CVF ≥40% del valor predicho
- DLco 30-89% del valor predicho
Medicación permitida durante el estudio:1
- Uso de prednisona ≤10mg/día.
- Tratamiento estable con micofenolato (mofetilo sódico) o metotrexato, durante ≥ 6 meses previos a la aleatorización.
- En los casos de deterioro clínicamente significativo durante el ensayo, se permitió un tratamiento adicional.†
Variables del estudio1
Variable principal
- Tasa anual de declive de la capacidad vital forzada (CVF) ml/año durante 52 semanas.
Variables secundarias principales
- Cambio absoluto respecto al periodo basal en el Índice cutáneo modificado de Rodnan (mRSS) a la semana 52.
- Cambio absoluto respecto al periodo basal en la puntuación total del cuestionario respiratorio del Hospital St. George (SGRQ) a la semana 52.
Características basales1
Las características basales fueron similares entre ambos grupos de tratamiento.1
Alrededor de tres cuartas partes de los pacientes eran mujeres, y la edad media era de 54 años. El 51,9% de los pacientes presentaba esclerosis sistémica difusa.1
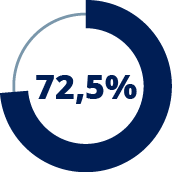
Valor medio del %CVF predicho
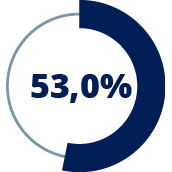
Valor medio del %DLco predicho
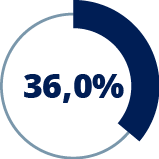
Extensión media de fibrosis en la TCAR
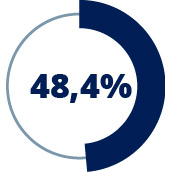
de los pacientes tomaba micofenolato de base
Principales resultados del estudio1
El tratamiento con nintedanib redujo de forma significativa la tasa ajustada anual de declive de la CVF durante 52 semanas frente a placebo (diferencia 41,0 ml/año, IC 95%: 2,9 – 79,0; p=0,04). La reducción relativa en la tasa anual de declive de la CVF entre nintedanib y placebo fue del 44%, similar al porcentaje de reducción relativa observado en los ensayos clínicos INPULSIS 1 y 2 (49%).1,4
Tasa anual de declive de la CVF (ml/año)1
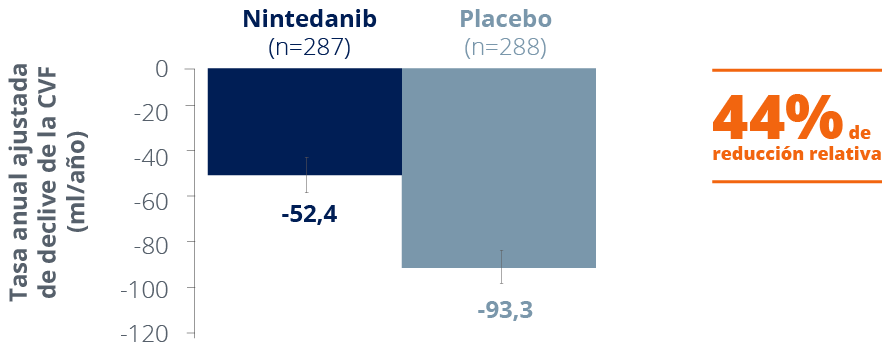
La tasa anual de declive de la CVF durante 52 semanas fue menor en el grupo tratado con nintedanib frente al grupo tratado con placebo (-52,4 ml/año vs. −93,3 ml/año).1
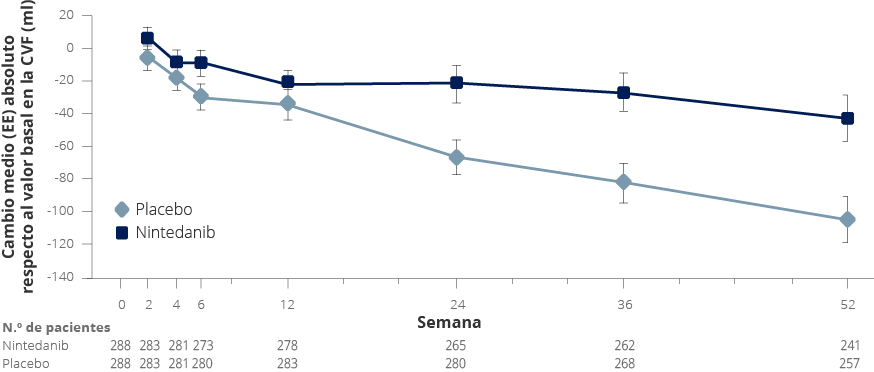
Las curvas del cambio respecto al valor basal en la CVF (ml) se separaron claramente en la semana 12 y siguieron divergiendo hasta la semana 52.1
Tasa anual de declive de la CVF (ml/año)1
Otros resultados de eficacia1
La reducción en el declive de la CVF en el grupo tratado con nintedanib no se acompañó de una mejora en la calidad de vida relacionada con la salud.
No se observó ningún efecto sobre la fibrosis cutánea, evaluada mediante el índice cutáneo modificado de Rodnan (mRSS).
Resultados de seguridad1
La diarrea fue el evento adverso más frecuente en ambos grupos del ensayo (75,7% en el grupo nintedanib y 31,6% en el grupo placebo).
El perfil de seguridad y tolerabilidad de nintedanib en este ensayo fue consistente con el observado en el ensayo INPULSIS®.1,4
Los resultados del ensayo SENSCIS® muestran que nintedanib tiene un efecto beneficioso al reducir la tasa de declive de la CVF en pacientes con EPI-ES durante 1 año.1
*Según los criterios del ACR/EULAR de 2013 y con <7 años de evolución desde la primera manifestación diferente de Raynaud.3 †Los tratamientos adicionales (por lo demás, restringidos) permitidos fueron micofenolato de mofetilo, micofenolato sódico, metotrexato, azatioprina, ciclofosfamida, ciclosporina A, >10mg/día de prednisona, hidroxicloroquina, colchicina, D-penicilamina, sulfasalazina, rituximab, tocilizumab, abatacept, leflunomida, tacrolimus y nuevos tratamientos antiartríticos como tofacitinib y paraaminobenzoato potásico.
A: aleatorización; bid: dos veces al día; CVF: capacidad vital forzada; DLco: capacidad de difusión pulmonar del monóxido de carbono; EPID: enfermedad pulmonar intersticial difusa; EPI-FP: enfermedad pulmonar intersticial asociada a esclerosis sistémica; ES: esclerosis sistémica; IC: intervalo de confianza; mRSS: Índice cutáneo modificado de Rodnan; SGRQ: cuestionario respiratorio del Hospital St. George; TCAR: tomografía computarizada de alta resolución.
Referencias
- Distler O, et al. Nintedanib for Systemic Sclerosis-Associated Interstitial Lung Disease. N Engl J Med. 2019;380(26):2518-2528.
- Distler O, et al. Design of a randomised, placebo-controlled clinical trial of nintedanib in patients with systemic sclerosis-associated interstitial lung disease (SENSCIS™). Clin Exp Rheumatol. 2017;35(Suppl 106):75-81
- van den Hoogen F, et al. Classification criteria for systemic sclerosis: an American College of Rheumatology/European League against Rheumatism collaborative initiative. Ann Rheum Dis 2013;72(11):1747-55.
- Richeldi L, et al. Efficacy and safety of nintedanib in idiopathic pulmonary fibrosis. N Engl J Med. 2014;370(22):2071-82.
ILD.0480.122021
